Het gehoor-foutje in mijn genen ge-pinpoint
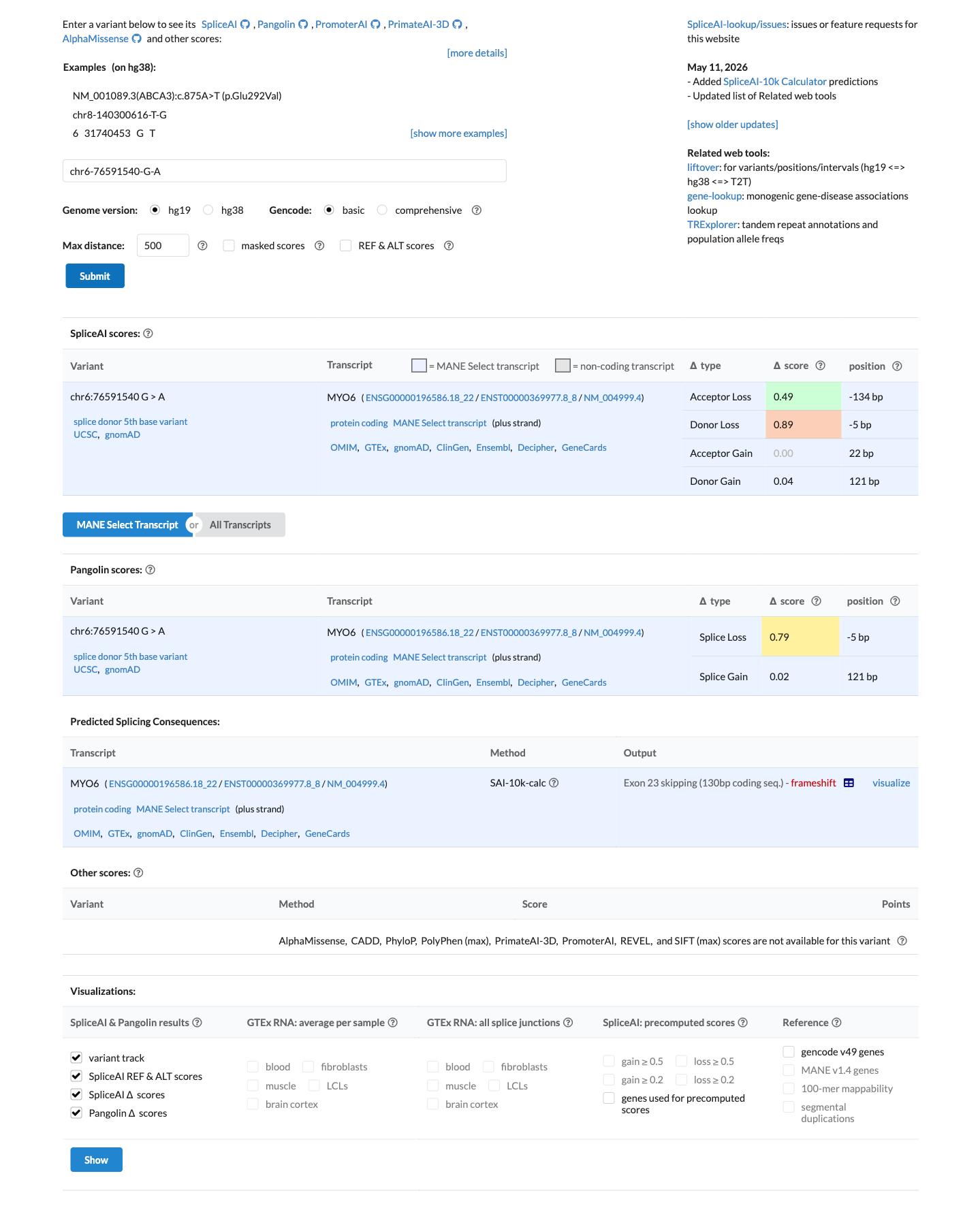
Na ruim een maand wachten kon ik mijn complete dna downloaden. De analyse-pijplijn had ik ondertussen al gebouwd (en een crash-course klinische genetica gevolgd). Na een marathon-sessie op hemelvaartsdag is er één serieuze kandidaat voor mijn slechte gehoor: MYO6 c.2416+5G>A, een novel splice-variant in intron 23. Afwezig in gnomAD (0 dragers op 280.000+ samples), novel in ClinVar, en pal naast twee bekende Likely Pathogenic varianten in dezelfde splice-donor. In-silico ondersteund door SpliceAI (Donor Loss 0,89) en Pangolin (0,79). Beide wijzen op exon-skipping → frameshift → haploinsufficiëntie. Een comprehensive tweede pass tegen het DVD v9.2-panel (224 genen) leverde geen alternatief op.
Op 14 mei verstuurd: een mail aan dr. M. Kriek (LUMC Klinische Genetica, stelde de DFNA22-diagnose in 2020) met voorstel voor Sanger-bevestiging, ClinVar-co-submission en een case report. Op 15 mei opgesteld: de eerste gentherapie-ontwerpbrief — target product profile voor deze specifieke variant.
Status: kandidaat-variant, in-silico ondersteund. Sanger en RNA-studie zijn de volgende validatiestappen.
Recente ontwikkelingen
De afgelopen weken in mijn onderzoek en in de bredere gehoor-gentherapie wereld.
Gentherapie-ontwerpbrief opgesteld + RNA-studie-route uitgewerkt
Eerste target product profile voor c.2416+5G>A: payload, promoter, AAV-serotype, intracochleaire toediening, en een beslisboom die afhangt van de RNA-uitslag. GTEx-check: patiënt-RNA voor de splicing-studie haalbaar vanaf huidbiopt (fibroblasten ~15 TPM) of LCL (~19 TPM), niet vanaf vol bloed. Edward Dolk bood aan de Sanger-bevestiging 's avonds in zijn lab te doen.
Kandidaat-variant geïdentificeerd: MYO6 c.2416+5G>A
WGS-analyse op 79 gehoor-genen, daarna comprehensive tweede pass tegen DVD v9.2 (224 genen) — één kandidaat, geen alternatief. In-silico (SpliceAI 0,89, Pangolin 0,79) wijst op exon-skipping → frameshift → haploinsufficiëntie. Mail naar dr. Kriek (LUMC) verzonden voor Sanger-bevestiging en ClinVar-co-submission.
Otarmeni continued approval — endpoints gezet voor cochleaire AAV-trials
Otarmeni's continued approval is contingent op durability en speech-development metrics in de confirmatory CHORD-fase. Dat zet de standaard waar toekomstige cochleaire AAV-approvals (ook MYO6) aan moeten voldoen. Plus: FDA Public Meeting CNPV op 4 juni 2026 — kanaal voor patient-input.
🏛️ FDA-approval Otarmeni — eerste cochleaire AAV-gentherapie ooit
Regeneron's lunsotogene parvec-cwha goedgekeurd voor biallelische OTOF-varianten. CHORD-trial: 80% ≤70 dB HL @ 24 wk, 42% normaal gehoor (≤25 dB) @ 48 wk. Regulatory anchor voor de MYO6-route: accelerated-approval-template, intracochleaire AAV bewezen veilig in mensen, Myo15-promoter blueprint.
Nature: AAV1-hOTOF n=42 — 90% gehoorherstel tot 2,5 jaar
Multicentre publicatie (Jiang/Cheng/Lv/Shu et al.). Eerste menselijke OTOF-gentherapie-paper met grote N en lange follow-up. Yilai Shu (Fudan, dé MYO6-gentherapie-lab) is co-lead — top contact-kandidaat na Sanger-bevestiging.
Wie ben ik, wat heb ik
Onno ter Wisscha, 56, Utrecht. Ernstig slechthorend sinds mijn 10e à 12e jaar (na een oorontsteking), met een ski-slope-patroon: rond de 50 dB verlies op 250 Hz, aflopend naar geen waarneembaar gehoor boven 3200–3500 Hz. Stabiel van mijn 13e tot ongeveer mijn 50e; sindsdien lichte verslechtering.
In juni 2020 stelde dr. M. Kriek (LUMC Klinische Genetica) de diagnose DFNA22 vast — autosomaal-dominant gehoorverlies veroorzaakt door een mutatie in het MYO6-gen. Vier generaties in de familie aangedaan; mijn dochter hoort goed (vastgesteld op haar 18e, alleen via audiogram — Sanger-test op de variant is nog niet gedaan).
Geen vestibulaire klachten. Geen syndromale kenmerken. Hoortoestellen vanaf mijn 13e, nu Oticon Intent 1.
Vier sporen parallel
Niet wachten op één route — vier sporen tegelijk volgen, met verschillende tijdshorizons en risico-profielen.
Gerichte MYO6-gentherapie
Gene augmentation via AAV. Variant geïdentificeerd; in-silico ondersteund; mail naar LUMC verzonden. Otarmeni (apr 2026) is de regulatory anchor. Volgende stap: RNA-/minigene-studie om haploinsufficiëntie functioneel te bevestigen.
Epigenetische herprogrammering
Partiële Yamanaka-reprogramming (PER) — adresseert mogelijk de leeftijdsgerelateerde verslechtering. Life Biosciences ER-100 in trial voor oog; Retro Biosciences RTR242 Q3 2026.
CIRBP / DNA-reparatie (walvis-route)
Versterkte DNA-reparatie via walvis-CIRBP zou cochleaire schade kunnen beperken. Genflow SLAB-trial (SIRT6 in honden): trial-afronding eind juli 2026, complete data augustus.
Brain-Computer Interface
Directe stimulatie van de auditieve cortex — bypassed oor én zenuw. Pas relevant als A/B/C onvoldoende opleveren. Neuralink Blindsight als precedent voor zicht; nog geen auditory-cortex programma.
Tijdlijn
Persoonlijke voortgang, onderzoeks-mijlpalen en relevante ontwikkelingen in de buitenwereld — in één stroom.
MYO6-dossier — variant & gentherapie-ontwerp
De technische kern: wat is c.2416+5G>A precies, en hoe zou een therapie eruit kunnen zien?
ACMG-classificatie
De variant ligt in dezelfde splice-donor-consensus als c.2416+1G>A en c.2416+2T>C, beide Likely Pathogenic in ClinVar. SAI-10k voorspelt expliciet exon 23 skipping → frameshift → premature stopcodon → nonsense-mediated decay. Toegepaste criteria: PVS1 (gereduceerd, predictie-gebaseerd) + PM2_Supporting + PP3_Supporting, met PM1 mogelijk als Moderate gezien de directe nabijheid van twee LP-buren. Dat tilt de variant van VUS naar de grens van Likely Pathogenic. RNA-bevestiging van het skipping-mechanisme zou PVS1 naar Strong tillen en de classificatie definitief op LP/Pathogenic zetten.
Gentherapie-ontwerpbrief — wat het is, wat het niet is
Wat het niet is: een buildbare specificatie, of een belofte van een vector op korte termijn. Eerste MYO6-trial is realistisch 2028–2032. Bespoke n-of-1-therapieën bestaan (Milasen-precedent), maar kosten miljoenen en gaan vrijwel altijd over fatale kinderziekten.
Wat het wél is: een target product profile dat alle ontwerp-parameters voor c.2416+5G>A op één plek zet, met expliciete aannames en open vragen. Drie doelen: (1) werkdocument dat meegroeit met nieuwe data, (2) overdraagbaar stuk voor Shu, Kriek, Rutten, (3) pipeline-positionering — als MYO6-trials starten, is deze variant gekarakteriseerd en Onno aangehaakt.
Ontwerp-parameters (mits haploinsufficiëntie bevestigd)
- Strategie: gene augmentation (AAV gene addition) — geen silencing nodig. Otarmeni-blauwdruk.
- Payload: MYO6 CDS ~3855 bp; AAV-capaciteit ~4,7 kb incl. ITRs/promoter/polyA — zeer krap. Single-AAV met minimale promoter, of dual-AAV (lagere efficiëntie).
- Promoter: hair-cell-specifiek (vergelijkbaar met Myo15-promoter in Otarmeni). Moet compact.
- Toediening: intracochleaire AAV-infusie via ronde venster — sinds Otarmeni bewezen veilig.
- Patiënt-specifiek: adult-onset (geen publieke MYO6-data voor volwassenen); ski-slope (hoge frequenties vermoedelijk reeds verloren); lage frequenties hebben restgehoor → het targetweefsel.
Trials & netwerk
De relevante klinische trials, onderzoekers en contacten waar dit veld op draait.
Klinische trials — gehoor-gentherapie (2026)
| Programma | Gen / target | Fase | Status |
|---|---|---|---|
| Otarmeni (Regeneron) | OTOF biallelisch | FDA-approved | 23 apr 2026 — eerste cochleaire AAV-gentherapie ooit |
| AAV1-hOTOF (Shu et al.) | OTOF | Trial n=42 | Nature 22 apr 2026 — 90% gehoorherstel tot 2,5 jr |
| SENS-501 AUDIOGENE (Sensorion) | OTOF | Phase 1/2 | 6-mnd data cohort 2 — aanhoudende efficacy, 3e cohort overwogen |
| SENS-601 (Sensorion) | GJB2 (recessief) | Preklinisch | ASGCT mei 2026 poster; CTA H1 2026, IND eind 2026 |
| Eli Lilly × Seamless | Programmable recombinase (HL) | Discovery | Target-genen nog niet publiek |
| MYO6-trial | MYO6 dominant | — | Geen lopend programma; realistisch 2028–2032 |
Onderzoeksnetwerk
dr. M. Kriek
Stelde DFNA22-diagnose vast (juni 2020). Primaire klinische route — mail 14 mei 2026 met c.2416+5G>A. Sanger-bevestiging + ClinVar-co-submission.
Prof. Yilai Shu
Leidende groep wereldwijd voor MYO6-editing. CRISPR-rescue C442Y muismodel (2021), dCas13X RNA base editing (2022). Co-lead op recente OTOF Nature-paper. Contacteren na Sanger.
Bert Rutten
Directe ervaring met ASO/RNA-therapeutica en trial design. Denkt mee over therapiestrategie; in CC op de LUMC-mail.
Edward Dolk
Bood 15 mei aan de Sanger-bevestiging 's avonds in zijn lab te doen — snelle parallelle pre-validatie naast LUMC.
Zheng-Yi Chen
Adult-editing en bredere gentherapie-toepassingen voor gehoor.
Jan de Laat
Eerder samengewerkt (Golden Hearing). Audiologische interpretatie en LUMC-netwerk.
Justin Makker
Vaste audicien, fitting en monitoring. Niet voor DPOAE — die staat alleen in academische ziekenhuizen.
Prof. Ronald Pennings
DOOFNL-cohort. Klinische-validatierol overgenomen door LUMC/Kriek-route.
Hoe kun je helpen?
Dit is een open notebook. De volgende stappen zijn concreet — en op verschillende manieren te ondersteunen.
RNA-/minigene-studie
De hoogste-prioriteit volgende stap. Een lab dat patiënt-RNA (huidbiopt of LCL) of een minigene-assay kan draaien om exon-skipping functioneel te bevestigen.
ClinVar-co-submission
Variant indienen als novel Likely Pathogenic — samen met LUMC. Bouwt de evidence-base voor toekomstige patiënten met dezelfde variant.
Patient registries
Aansluiting bij internationale DFNA22-registries, Matchmaker Exchange, GeneMatcher, of ERN-netwerken — voor cosegregatie en cohort-vorming.
Doorverwijzingen
Ken je iemand in gentherapie-onderzoek, audiogenetica, of cochleaire AAV-trials? Een introductie helpt — vooral richting Yilai Shu / Fudan, of Europese AAV-centra.
Gehoorverlies in de familie?
Als jij of familieleden ook gehoorverlies hebben, kan genetisch onderzoek waardevol zijn. Vraag je huisarts of geneticus naar WGS of een gehoor-genen-paneel.
Deel deze pagina
Bouw mee aan dit netwerk. Elk paar ogen op deze pagina kan een deur openen. Volledige WGS-data, audiogrammen en methodologie beschikbaar op verzoek.
Ik sta open voor klinische consultatie, samenwerking, of verwijzingen
Volledige WGS-data (VCF + FASTQ), audiologische records, en methodologie-rapporten zijn beschikbaar op verzoek.
onno@terwisscha.com